下列框表中的A--L中是中学化学中常见的物质,所有物质均由短周期元素组成.已知常温、常压下,C为无色液体,D、E、L均为气体单质,H是一种可溶于盐酸和氢氧化钠溶液的白色固体,J是具有强氧化性的一元弱酸,A--L可发生如下转化:
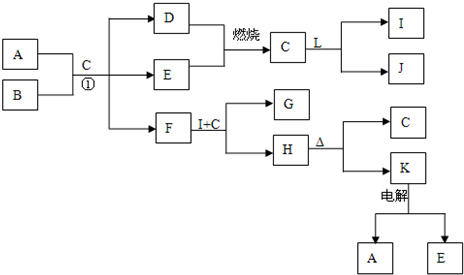
请回答下列问题:
(1)J的电子式______
(2)写出C、L反应转化为I和J的离子方程式______
(3)H是一种用于治疗胃酸过多的药物的主要成分,其治疗原理用离子方程式表示______
(4)写出F与I、C转化为G和H的离子方程式______
(5)如果A、B的物质的量之比为2:1,写出①的化学反应方程式______.
常温、常压下,C为无色液体,应为H2O,则D、E为H2、O2中的一种,J是具有强氧化性的一元弱酸,应为HClO,则L为Cl2,I为HCl,H是一种可溶于盐酸和氢氧化钠溶液的白色固体,且能加热分解,则H为Al(OH)3,K为Al2O3,电解生成的E为O2,所以D为H2,F能和盐酸反应生成Al(OH)3,则F为NaAlO2,所以B为Na2O2,A、B和水混合时,分别生成H2、O2、NaAlO2,
NaAlO2和盐酸反应生成Al(OH)3和NaCl,则G为NaCl,则
(1)J是具有强氧化性的一元弱酸,应为HClO,电子式为
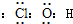
,故答案为:
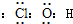
;
(2)氯气和水反应生成盐酸和次氯酸,其中次氯酸为弱酸,反应的离子方程式为Cl2+H2O=H++Cl-+HClO,
故答案为:Cl2+H2O=H++Cl-+HClO;
(3)Al(OH)3具有两性,与酸反应生成盐和水,反应的离子方程式为Al(OH)3+3H+=Al3++3H2O,
故答案为:Al(OH)3+3H+=Al3++3H2O;
(4)NaAlO2和盐酸反应生成Al(OH)3和NaCl,反应的离子方程式为AlO2-+H++H2O=Al(OH)3↓,
故答案为:AlO2-+H++H2O=Al(OH)3↓;
(5)如果A、B的物质的量之比为2:1,根据元素质量守恒,可写出反应方程式为2Na2O2+4Al+6H2O=4NaAlO2+6H2↑+O2↑,
故答案为:2Na2O2+4Al+6H2O=4NaAlO2+6H2↑+O2↑.
