生活离不开金属.
(1)“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠和水等,其发热原理是利用铁生锈时放热,发热剂需与空气中______接触才会发热.
(2)已知下列各组物质间均能发生反应
A.Fe和CuSO4溶液B.Mg和MnSO4溶液C.Mn和FeSO4溶液
①写出Fe和CuSO4溶液反应的化学方程式______.
②Mn、Fe、Mg、Cu四种金属的活动性由强到弱的顺序______.
(3)化学小组在实验结束后,进行了如下废液处理: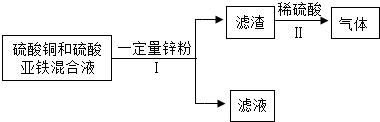
①Ⅰ中的操作名称是______.
②写出Ⅱ中一定发生反应的化学方程式______.
③滤液的组成可能是______.
(1)铁在有水和氧气并存时易生锈,根据发热剂提供的物质可以知道,铁要生锈还需要氧气,
故填:氧气;
(2)铁和硫酸铜能反应生成硫酸亚铁和铜,Fe和CuSO4 溶液能反应说明Fe>Cu,Mg和MnSO4 溶液能反应说明Mg>Mn,Mn和FeSO4 溶液能反应说明Mn>Fe,故这四种金属的活动性顺序为Mg>Mn>Fe>Cu,
故填:Mg>Mn>Fe>Cu;
(3)经过操作I得到滤液和滤渣,故该操作为过滤,锌能与硫酸铜反应生成硫酸锌和铜,锌能与硫酸亚铁反应生成铁和硫酸锌,故滤液中一定含有硫酸锌,向滤渣中加入稀硫酸能产生气体,说明滤渣中一定含有铁,故一定会发生铁和硫酸的反应,铁能和硫酸反应生成硫酸亚铁和氢气,由于滤渣中含有铁,故滤液中一定不含有硫酸铜,当加入的锌粉只与一部分硫酸亚铁反应时,滤液中含有硫酸亚铁,
故填:Ⅰ、过滤;
Ⅱ、Fe+H2SO4═FeSO4+H2↑;
Ⅲ、ZnSO4或ZnSO4和FeSO4的混合物(答不全不得分).
