图中X、Y、Z为单质,其它为化合物,它们之间存在如图转化关系(部分产物已略去).其中,A俗称磁性氧化铁;E是不溶于水的酸性氧化物,能与氢氟酸反应.
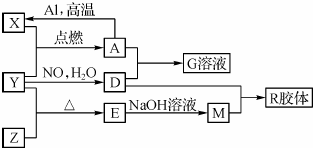
回答下列问题:
(1)组成单质Y的元素在周期表中的位置是______;M中存在的化学键类型为______;R的化学式是______.
(2)一定条件下,Z与H2反应生成ZH4,ZH4的电子式为______.
(3)已知A与1molAl反应转化为X时(所有物质均为固体).放出aKJ热量.写出该反应的热化学方程式:______.
(4)写出A和D的稀溶液反应生成G的离子方程式:______.
A俗称磁性氧化铁,即为四氧化三铁;能与氢氟酸反应且不溶于水的酸性氧化物是SiO2,即E为SiO2,根据框图中的转化关系,可知X为铁、Y为O2、Z为Si、D为硝酸、M为硅酸钠、G为硝酸铁,R为H2SiO3;
(1)根据氧原子的核外电子排布,知氧元素在周期表的第二周期第VIA族;硅酸钠中有离子键、共价键;R的化学式是
H2SiO3(或H4SiO4);故答案为:第二周期第VIA族;离子键、共价键; H2SiO3(或H4SiO4);
(2)ZH4的分子式为SiH4,其电子式为:
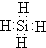
,故答案为:
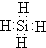
;
(3)根据热化学方程式的书写方法和书写原则,反应的热化学方程式为8Al(s)+3Fe3O4(s)=9Fe(s)+4Al2O3(s)△H=-8a kJ/mol;
故答案为:8Al(s)+3Fe3O4(s)=9Fe(s)+4Al2O3(s)△H=-8a kJ/mol;
(4)四氧化三铁和硝酸反应是氧化物中的二价铁元素被氧化到最高价,硝酸中氮元素被还原到+2价,反应的离子方程式为:3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O;
故答案为:3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O
