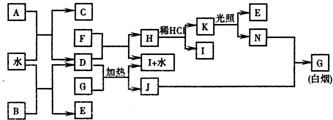
下图为某些常见物质之间的转化关系.已知:A、B、I中含有相同的阳离子且都是XY2型化合物,且I是实验室常用的干燥剂;C为直线型分子;E、F为非金属气体单质.
请按要求填空:
(1)①B的电子式是______,②K的结构式是______;
(2)D与G反应的化学方程式是______;
(3)已知C的燃烧热是1300kJ/mol,表示C的燃烧热的热化学方程式是______;
(4)将G溶于水配成溶液,简述检验该溶液G中所含阳离子的操作方法:______;
(5)常温下0.1mol/L的J溶液中c(H+)/c(OH-)=1×10-8,下列叙述错误的是______;
A.该溶液的pH=11;
B.该溶液中的溶质电离出的阳离子浓度0.1mol/L
C.该溶液中水电离出的c(H+)与c(OH-)乘积为1×10-22
D.pH=3的盐酸溶液V1 L与该0.1mol/L的J溶液V2 L混合,若混合溶液pH=7,则:V1>V2
E.将以上溶液加水稀释100倍后,pH值为9;
(6)单质F在工业上有重要的用途是______.(至少两种)
根据题意“C为直线型分子”,从框图可以看出C是A和水反应生成的,可以初步确定C是乙炔,则A为碳化钙,D是氢氧化钙,框图中的G(白烟),中学学过的就是氯化铵,以两条线索为切入点,推知其他物质分别为:B是CaO2,E是氧气,F是氯气,G是难溶碱如氢氧化铁、氢氧化铜等,H是次氯酸钙,I是氯化钙、J是氯化铁等、K是次氯酸,N是HCl.
(1)①过氧化钙是离子化合物,电子式为:
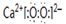
,故答案为:
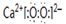
;
②次氯酸是共价化合物,氢元素、氯元素以及氧元素均达到了稳定结构,结构式为:H-O-Cl,故答案为:H-O-Cl;
(2)实验室中利用氯化铵和氢氧化钙反应来制取氧气,反应原理为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O, △ .
故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O; △ .
(3)燃烧热实指1ml可燃物燃烧生成最稳定的氧化物释放出的能量,所以乙炔燃烧的方程式为:C2H2(g)+
O2(g)=2CO2(g)+H2O(l)△H=-1300kJ/mol,5 2
故答案为:C2H2(g)+
O2(g)=2CO2(g)+H2O(l)△H=-1300kJ/mol;5 2
(4)铵根离子的检验原理是:铵根离子和强碱在加热的条件下生成能使湿润的红色石蕊试纸变蓝的氨气,
故答案为:取少量的氯化铵溶液于试管中,加入适量的氢氧化钠溶液,加热试管,将湿润的红色石蕊试纸放在试管口,若试纸变成蓝色,则含有NH4+;
(5)A、0.1mol/L的氯化铁溶液中,c(H+)/c(OH-)=1×10-8,c(H+)•c(OH-)=10-14,所以c(H+)=10-11mol/L,即该溶液的pH=11,故A正确;
B、0.1mol/L的氨水溶液中,因为一水合氨是弱电解质,不完全电离,铵根离子的浓度小于0.1mol/L,故B错误;
C、常温下,该溶液中水电离出的c(H+)与c(OH-)乘积为1×10-14,温度不变,数值不变,故C错误;
D、pH=3的盐酸溶液V1 L与该0.1mol/L的氨水溶液V2 L混合,若混合溶液pH=7,则需要酸过量,则:V1>V2,故D正确;
E、一水合氨是弱电解质,加水稀释100倍后,pH值大于9,故E错误.
故选BCE;
(6)氯气的工业用途:制漂白粉,制盐酸(制制漂白液等),故答案为:制漂白粉,制盐酸(制漂白液等).
