短周期元素形成的纯净物A、B、C、D、E之间的转化关系如图1所示,物质A与物质B之间的反应不在溶液中进行(E可能与A、B两种物质中的某种相同).
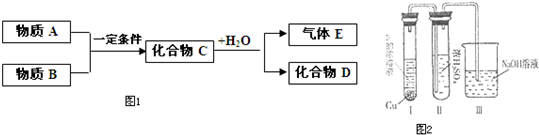
请回答下列问题:
(1)若C是离子化合物,D是一种强碱,写出C的化学式______.
(2)若E是有臭鸡蛋气味的气体硫化氢(其水溶液为二元弱酸),D是既能溶于强酸、又能溶于强碱的化合物.
用等式表示E与NaOH溶液反应后生成正盐的溶液中所有离子浓度之间的关系______.
(3)若C是一种红棕色气体,D是一种强酸,则:
①C与水反应的化学方程式为______.
②有人认为“浓H2SO4可以干燥气体C”.某同学为了验证该观点是否正确,用右图装置进行实验(反应前Ⅰ、Ⅱ装置中空气已排尽).实验进行一段时间后,浓H2SO4中未发现有气体逸出,且该溶液变为红棕色,则你得出的结论是______.
③已知A与物质B及水作用生成D,写出此反应的化学方程式______.
(1)若C是离子化合物,D是一种强碱,可能为NaOH,则C可为Na2O2(或NaH),生成气体为O2或H2,故答案为:Na2O2(NaH);
(2)若E是有臭鸡蛋气味的气体硫化氢(其水溶液为二元弱酸),应为H2S,D是既能溶于强酸、又能溶于强碱的化合物,应为Al(OH)3,则C为Al2S3,
E与NaOH溶液反应后生成正盐为Na2S,溶液中存在电荷守恒,为c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-),
故答案为:c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-);
(3)C是有色气体,应为NO2,则D为HNO3,E为NO,
①NO2与水反应生成HNO3和NO,反应的方程式为3NO2+H2O=2HNO3+NO,故答案为:3NO2+H2O=2HNO3+NO;
②由现象实验过程中,浓H2SO4中未发现有气体逸出,且浓H2SO4由无色变为红棕色,可以得出NO2能溶于浓硫酸中,
故答案为:NO2能溶于浓H2SO4,因而不能用浓H2SO4干燥NO2;
③A和B的反应应为NO和O2的反应,在溶液中发生4NO+3O2+2H2O=4HNO3,
故答案为:4NO+3O2+2H2O=4HNO3.
