(10菏泽14)、学习金属单元后,小强知道了铁是当今世界用量最多的金属,而每年全世界被腐蚀损耗的钢铁材料,约占全年钢产量的十分之一。于是小强对金属铁的相关知识开展了探究性学习。
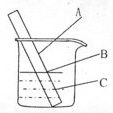
(1)如图,小强将一根20cm的光亮的铁棒放在自来水中,观察A、B、C三处的变化。几天后,他发现_________(填序号)处最先出现铁锈,小强结合书本知识知道,铁生锈实际是铁和________、__________等物质发生反应的过程。
(2)小强来到已停产的企业厂房,看到许多机械设备上已锈迹斑斑,他马上想到可以用稀盐酸将铁锈(主要成分Fe2O3)除去,该反应的化学方程式为:______________________
去锈后为防止机械设备进一步锈蚀,小强想到的一种防护方法是_______________________
_______________________。
B, 氧气、水(或者 O2 H2O) Fe2O3+6HCl==2FeCl3+3H2O 涂油、刷漆等
本题考查的是探究金属锈蚀的条件。
(1)根据钢铁生锈的条件是钢铁与氧气和水同时接触,B处满足条件,故先生锈;钢铁的锈蚀主要是铁与空气中的氧气、水蒸气等物质发生化学反应的结果。
(2)盐酸和铁锈(主要成分Fe2O3)反应,生成氯化铁和水,故反应的化学方程式为Fe2O3+6HCl==2FeCl3+3H2O;防止金属锈蚀就是防止金属与氧气或水接触,方法有制成不锈钢、在金属表面涂油、漆等。
