下列框图中的A-G是中学化学中常见的七种物质,已知常温、常压下D为无色液体,C、E为气态单质,B为金属单质,其它为化合物,A、G、F焰色反应都显黄色.A-G可发生如下转化:

请填写下列空白:
(1)A的化学式为______,金属B原子结构示意图为______.
(2)写出B与G溶液反应的化学方程式______;若81gB与足量的G溶液完全反应,则转移的电子的物质的量为______;
(3)向F的水溶液中通入足量的CO2气体,其离子方程式为______.
框图中的A-G是中学化学中常见的七种物质,C、E为气态单质,二者在点燃条件下生成常温、常压下D为无色液体,则D为H2O,C、E分别为H2、O2中的一种,化合物A、G、F焰色反应都显黄色,均含有Na元素,A与水反应生成生成E与G,故A为Na2O2,E为O2,G为NaOH,可推知C为H2,金属B与NaOH溶液反应生成氢气与F溶液,则B为Al,F为NaAlO2,过氧化钠与Al加水,可以得到氢气、氧气与偏铝酸钠,
(1)由上述分析可知,A为Na2O2,B为Al,原子核外有3个电子层,各层电子数为2、8、3,其原子结构示意图为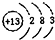 ,
,
故答案为:Na2O2;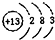 ;
;
(2)Al与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应的化学方程式为:2NaOH+2Al+2H2O═2NaAlO2+3H2↑,81gAl的物质的量=
=3mol,与足量的NaOH溶液完全反应,则转移的电子的物质的量为3mol×3=9mol,81g 27g/mol
故答案为:2NaOH+2Al+2H2O═2NaAlO2+3H2↑;9mol;
(3)向NaAlO2的水溶液中通入足量的CO2气体,反应生成氢氧化铝沉淀与碳酸氢钠,其离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
故答案为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.
