问题
计算题
(1)计算燃烧产物中水的质量。
(2)若原气体是单一气体,通过计算推断它的分子式。
(3)若原气体是两种等物质的量的气体的混合物,其中只有一种是烃,请写出它们的分子式(只要求写出一组)。
答案
(1)2.7 g (2)C2H4 (3)C4H6和H2(或“C3H6和CO”“C3H6和CH2O”等)
(1)m(CO2)=15.0 g×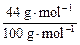 =6.6 g
=6.6 g
m(CO2+H2O)=9.3 g m(H2O)=9.3 g-6.6 g=2.7 g
(2)n(CO2)=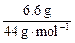 =0.15 mol n(H2O)=
=0.15 mol n(H2O)=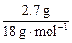 =0.15 mol
=0.15 mol
分子中C∶H=1∶2
n(无色可燃气体)=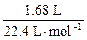 =0.075 mol
=0.075 mol
分子中C原子数=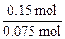 =2,分子中氢原子数=2×2=4
=2,分子中氢原子数=2×2=4
所以该气体的分子式是C2H4。
(3)因为单一气体为C2H4,现为等物质的量的两种气体之混合物,所以在2 mol混合气体中,应含有4 mol C原子,8 mol H原子,这两种气体可能是C4H6和H2(或“C3H6和CO”“C3H6和CH2O”等)。
