(6分)工业上用硫铁矿石(主要成分FeS2)在沸腾炉中焙烧,经过一系列反应,得到硫酸。焙烧后的矿渣用于炼铁。其转化过程如下(部分条件和产物已略去)。
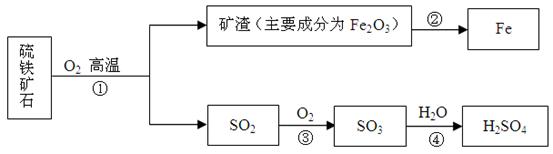
请回答下列问题:
(1)上图出现的含硫元素的物质中,属于氧化物的有 (填化学式)。
(2)FeS2中的铁元素是+2价,硫元素的化合价为 。
(3)写出②处炼铁的化学方程式 。若用2000 t含杂质30%的矿渣炼铁,理论上可得到含铁98%的生铁质量为_________ t。
(4)在煤炭燃烧过程中也会产生SO2。工业上将煤燃烧产生的烟气通入吸收塔,用石灰水淋洗,外加氧气的作用,使之反应生成硫酸钙和水。请写出该反应的化学方程式 。
(1)SO2、SO3
(2)-1
(3)3CO + Fe2O3 2Fe + 3CO2 1000 (2分)
2Fe + 3CO2 1000 (2分)
(4)2SO2 + 2Ca(OH)2 + O2 ="===" 2CaSO4 + 2H2O
题目分析:(1)上图出现的含硫元素的物质中,属于氧化物的有SO2、SO3。
(2)FeS2中的铁元素是+2价,硫元素的化合价为-1价。
(3)②处炼铁的化学方程式为:3CO + Fe2O3 2Fe + 3CO2。
2Fe + 3CO2。
[解]设若用2000 t含杂质30%的矿渣炼铁,理论上可得到含铁98%的生铁质量为X。
3CO + Fe2O3 2Fe + 3CO2
2Fe + 3CO2
160 112
2000t×30% X·98%
160:112=(2000t×30%):(X·98%)
X=1000t
答:若用2000 t含杂质30%的矿渣炼铁,理论上可得到含铁98%的生铁1000t。
(4)用石灰水淋洗,外加氧气的作用,使二氧化硫反应生成硫酸钙和水的化学方程式为:2SO2 + 2Ca(OH)2 + O2 ="===" 2CaSO4 + 2H2O。
点评:氧化物是指由氧元素和别的一种元素组成的化合物;书写化学方程式要遵循客观事实和质量守恒定律两个原则,注意化学式要正确,不要忘记反应条件、气体或者沉淀符号。
根据化学方程式计算,要注意解题的步骤,设、写、找、列、解、答。

