如图为中学常见物质间的转化关系,其中甲、乙、丙、丁为单质,其余为化合物,甲单质所含元素最外层电子数等于周期数,C常温下为无色液体,B焰色反应为黄色.一些在溶液中进行的反应溶液中的H2O及生成的H2O已省略.回答下列问题:
(1)单质乙所含元素在周期表中的位置______.
(2)化合物F的电子式______.
(3)D和G反应的离子方程式______.
(4)甲和A反应的化学方程式______.这类反应一般被称做______反应,该反应的主要应用______、______.
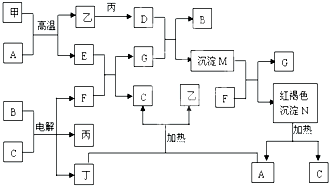
甲单质所含元素最外层电子数等于周期数,且为金属单质,能发生铝热反应,则甲是Al;
C常温下是无色液体,则H2O,红褐色沉淀N是Fe(OH)3,Fe(OH)3加热分解生成Fe2O3和H2O,A是Fe2O3,则乙是Fe、E是Al2O3,B焰色反应为黄色,则B中含有Na元素,B的水溶液电解生成三种物质,其中两种为单质、一种化合物,F能和氧化铝反应,则F是NaOH,铁能和丙反应,则丙是Cl2、丁是H2,G是NaAlO2,氯化铁和偏铝酸钠溶液反应生成Fe(OH)3、Al(OH)3沉淀和NaCl,
(1)乙是Fe,Fe位于第四周期第VIII族,故答案为:第四周期、Ⅷ族;
(2)F是NaOH,其电子式为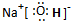 ,故答案为:
,故答案为: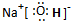 ;
;
(3)氯化铁溶液和偏铝酸钠溶液发生双水解反应生成氢氧化铁、氢氧化铝沉淀,离子方程式为:Fe3++3AlO2-+6H2O=Fe(OH)3↓+3Al(OH)3↓,故答案为:Fe3++3AlO2-+6H2O=Fe(OH)3↓+3Al(OH)3↓;
(4)铝和氧化铁在高温下发生置换反应,反应方程式为:2Al+Fe2O3
Al2O3+2Fe,该反应称为铝热反应,放出的大量热能使金属熔化,可以应用于焊接钢轨、冶炼难熔金属,高温 .
故答案为:2Al+Fe2O3
Al2O3+2Fe;铝热;焊接钢轨;冶炼难熔金属.高温 .
