某实验小组模拟高炉炼铁的化学反应原理进行实验,其装置如下图所示。
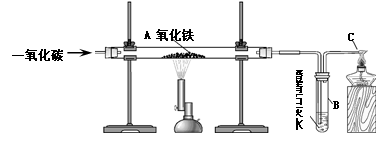
(1)A处发生反应的化学方程式是 。
(2)B中发生反应的化学方程式是 。
C处点燃酒精灯的目的是 。
(3)实验结束后,小李看到红色固体全部变黑了,认为产物就是单质铁,但小王提出了质疑:还有可能生成其它物质。为了进一步验证其固体成分,小王查到下列资料:①铁的氧化物有氧化铁、氧化亚铁、四氧化三铁(该化合物中铁有+2、+3两种化合价),其中氧化铁为红棕色,其余都为黑色;并且只有四氧化三铁能被磁铁吸引。②铁的氧化物都能与酸发生反应而溶解。③黄色的溶液:含有Fe3+的溶液(如氯化铁、硫酸铁、硝酸铁)
根据上述信息,小王又设计了两个实验。
[实验1]
将黑色固体研磨后,取少量加入 溶液中,观察到有气泡出现,溶液未变黄色,据此得出的结论是 。
[实验2]
再用磁铁吸引余下黑色固体,实验后即可对黑色固体成分进行判断:如果 ;如果 。
(1)3CO+Fe2O3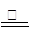 2Fe + 3CO2
2Fe + 3CO2
(2)CO2+Ca(OH)2= CaCO3↓ + H2O 防止CO污染环境
(3)稀硫酸(或稀盐酸) 有单质铁,无Fe3O4
如果黑色固体被磁铁全部吸引,说明只有单质铁;如果被部分吸引,说明黑色固体为Fe和FeO。
题目分析:一氧化碳还原氧化铁生成铁和二氧化碳,现象是红色的固体变成黑色,生成的二氧化碳能使澄清的石灰水变浑浊;剩余的尾气中含有一氧化碳,可通过燃烧法除去;
根据“观察到有气泡出现,溶液未变黄色”说明含有单质铁,不含氧化铁;再根据“只有四氧化三铁能被磁铁吸引”再用磁铁吸引余下黑色固体,实验后即可对黑色固体成分进行判断:若黑色固体被磁铁全部吸引,说明只有单质铁;如果被部分吸引,说明黑色固体为Fe和FeO。
