下列物质A~F是我们熟悉的单质或化合物,其中A、B是常见的金属,E在常温下是黄绿色气体;在适当的条件下,他们之间可以发生如图所示的转化.
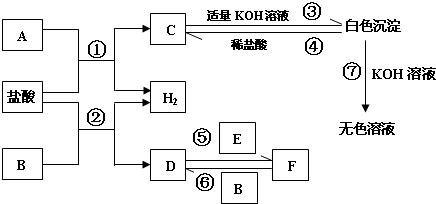
试回答下列问题:
(1)A的化学式是______;
(2)在①-⑦反应中,属于氧化还原反应的有______,其中属于置换反应的有______;
(3)写出上图中白色沉淀与NaOH溶液反应的离子方程式:______;
(4)请写出在D的溶液中滴加NaOH溶液的过程中发生反应的化学方程式______、______.
(5)检验上图无色溶液中金属阳离子的方法是(填写实验名称):______,现象是______.
A是常见的金属,由A+盐酸→C+H2,C为金属氯化物,C与KOH反应生成白色沉淀,可以溶于KOH、盐酸,故该白色沉淀为Al(OH)3,则C为AlCl3,A为Al.E在常温下是黄绿色气体,E为Cl2,由B+盐酸→D+H2可知,D为金属氯化物,D能与氯气反应生成F,F能与金属B反应得到D,则B为变价金属Fe,则D为FeCl2,F为FeCl3,FeCl3溶液可以与Fe反应生成FeCl2,
(1)由上述分析可知,A的化学式是Al,故答案为:Al;
(2)在①-⑦反应中,反应①②⑤⑥属于氧化还原反应,其中①②属于置换反应,
故答案为:①②⑤⑥;①②;
(3)图中白色沉淀为氢氧化铝,与NaOH溶液反应生成偏铝酸钠与水,离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)FeCl2溶液中滴加NaOH溶液的过程中发生反应的化学方程式:FeCl2+2NaOH=Fe(OH)2↓+2NaCl、4Fe(OH)2+O2+2H2O=4Fe(OH)3;
故答案为:FeCl2+2NaOH=Fe(OH)2↓+2NaCl;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(5)上图无色溶液中金属阳离子为K+,利用焰色反应进行检验,透过蓝色钴玻璃观察火焰颜色为紫色说明含有K+,
故答案为:焰色反应;透过蓝色钴玻璃观察火焰颜色为紫色.
