铜和铁是生产、生活中广泛使用的金属.
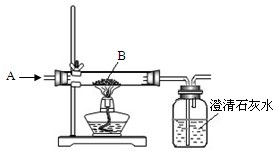
(1)下图是工业炼铁原理的实验示意图.气体A是______和红棕色粉末B是______.广口瓶中可观察到的现象是______;用化学方程式表示炼铁的反应原理是______;该实验中尾气的处理方法可以为______.
(2)铁生锈的条件是______;铜表面也容易生成绿色的铜锈,铜锈的主要成分是碱式碳酸铜,化学式为______.
(3)老师用生锈的铜片、铁粉和稀硫酸进行实验,实验过程如图所示(部分生成物己略去).
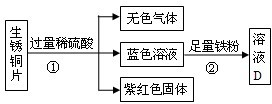
紫红色固体C的化学式为______.写出反应②中反应的化学方程式______.
(1)用一氧化碳还原红棕色的氧化铁粉末,同时生成二氧化碳,二氧化碳可以使澄清石灰水变浑浊,实验过程中未反应的一氧化碳有毒,不能直接排入空气中,可以将其点燃或收集起来.
故选CO Fe2O3澄清石灰水变浑浊 Fe2O3+CO
2Fe+3CO2点燃或用气球收集 高温 .
(2)铁在潮湿的空气中生锈生成铁锈,铜在潮湿的空气中也会生锈,生成铜绿,铜绿的主要成分是碱式碳酸铜,
化学式是Cu2(OH)2CO3
故答案为:与潮湿的空气接触 Cu2(OH)2CO3
(3)该实验流程为:生锈铜片表面的主要成分是 Cu2(OH)2CO3,它可以与硫酸反应生成二氧化碳无色气体、蓝色的硫酸铜溶液,当表面的铜锈反应完全后露出红色的铜;蓝色的硫酸铜溶液中还有未反应完的稀硫酸,所以向蓝色的硫酸铜溶液中加入铁粉时,铁既会与硫酸铜溶液反应又会与稀硫酸反应.
故选Cu Fe+CuSO4═FeSO4+Cu,Fe+H2SO4═FeSO4+H2↑