[化学——选修物质结构与性质](15分)
A、B、C、D是原子序数依次递增的短周期元素,四种元素的质子数之和小于23。
A元素原子的电子总数等于其基态原子的电子层数。B元素原子的价电子结构为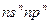 。C元素的第一电离能在同族元素中最大,并且高于同周期左右相邻的元素,但
。C元素的第一电离能在同族元素中最大,并且高于同周期左右相邻的元素,但
其单质的熔点却低于同周期左右相邻元素的单质。D的电负性大于C。
(1)B、C、D分别是 、 、 ;
(2)C、D分别与A形成的最简单分子中,稳定性较高的是 (填化学式)分子;该分子再与A+结合成离子时,ACA键的键角会发生改变,其原因是 。
(3)BD2分子的晶体结构为密堆积,则每个BD2分子周围紧邻的分子有 个;
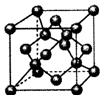
(4)上图为B元素的某种单质晶体X的晶胞,其中含有 个B原子,该晶体
(填“形成”或“没有形成”)最密堆积结构,原因是 。试分析比较晶体X与晶体BD2的熔点 。
(1)C、N、O(或碳、氮、氧)(每空1分)
(2)H2O(1分);H2O呈V形(键角约104.5°),H2O与H′形成配位键后,氧原子上
的孤对电子由两对变为一对,H—O——H的键角变大,H3O+呈三角锥形(或用杂化轨
道理解释)(2分)
(3)12(2分)
(4)8(2分);没有形成(1分);金刚石中每个碳原子以四个共价单键对称的与相邻的4个碳原子结合,C—C—C夹角为109°28′,形成空间网状结构(或答共价键具有方向性和饱和性)(2分);金刚石晶体是原子晶体,由固态转变为液态过程中要破坏共价键,所以熔点较高,干冰是分子晶体,由固态转变成液态过程中只破坏范德华力,所以熔点较低(2分)
