炼铁的原理可用化学方程式表示为Fe2O3+CO
Fe+CO2.某课外小组拟用下列装置做炼铁原理的实验.CO气体用乙二酸的分解反应(C2H2O4 高温 .
CO2+CO↑+H2O)来制备. 浓H2SO4 . △
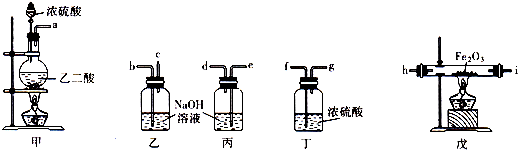
(1)为得到纯净的CO,并用来还原Fe2O3,则从甲装置中出来的混合气体经过上述装置的顺序应是(用乙、丙、丁、戊回答):[甲]→[______]→[______]→[______]→[______];用导管连接装置时(气流从左向右),应a连______,______连______,______连h,i连______.
(2)装置乙的作用是______;装置丙的作用是______.
(3)若实验后乙装置的质量增加m g,则参加反应的Fe2O3的质量为______g.
(1)在装置的连接中要注意先除杂后干燥,导气管的连接一般是长管进短管出,所以为得到纯净的CO,并用来还原Fe2O3,则从甲装置中出来的混合气体经过上述装置的顺序应是:[甲]→[丙]→[丁]→[戊]→[乙];用导管连接装置时(气流从左向右),应a连e,d连f,g连h,i连b;故填:丙;丁;戊;乙;e;d;f;g;b;
(2)氢氧化钠溶液能吸收二氧化碳,所以装置乙的作用是吸收反应中生成的二氧化碳;装置丙的作用是除去混合气体中的二氧化碳;故填:吸收反应中生成的二氧化碳;除去混合气体中的二氧化碳;
(3)装置乙中增加的质量就是生成二氧化碳的质量.
设参加反应的Fe2O3的质量为x.
Fe2O3+3CO
2Fe+3CO2 高温 .
160 132
x mg
=160 x 132 mg
x=
g40m 33
答:参加反应的Fe2O3的质量为
g.40m 33
