(6分)水是生命之源,饮用遭到污染的地下水不利于人体健康。政府积极建设自来水厂,让人们喝上清洁的水。
(1)测定地下水的酸碱度可用 。(填标号)
A.紫色石蕊溶液 B.无色酚酞溶液 C.pH试纸
(2)自来水生产过程中,可用 方法除去水中不溶性杂质,再通过活性炭层,利用其 性除去水中的颜色和异味,该过程属于 变化(填“物理”或“化学”)。
(3)ClO2是新一代饮用水的消毒剂,可以用来代替Cl2进行自来水的消毒。请回答下列问题:
①ClO2中“Cl”的化合价是 。
②制取ClO2的反应过程示意图如下:
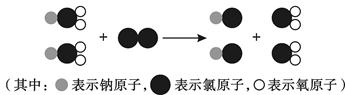
该反应的化学方程式为 。
(1)C(2)过滤;吸附;物理 (3)①+4②2NaClO2+Cl2→2NaCl+ 2ClO2
题目分析:(1)测定地下水的酸碱度可用pH试纸,选C。
(2)自来水生产过程中,可用过滤的方法除去水中不溶性杂质,再通过活性炭层,利用其活性炭的吸附性除去水中的颜色和异味,该过程属于物理变化。
(3)①ClO2中“Cl”的化合价是+4价。
②根据制取ClO2的反应过程示意图可知,该反应的化学方程式为2NaClO2+Cl2="2NaCl+" 2ClO2。
点评:过滤可以除去水中的固体不溶物;化合物中的各元素的化合价代数和为零;有新物质生成的反应是化学反应,没有新物质生成的反应是物理变化;书写化学方程式要遵循客观事实和质量守恒定律两个原则,注意化学式要正确,不要忘记反应条件、气体或者沉淀符号。

 B
B 
 D
D