问题
填空题
(14分)现有A、B、C、D四种物质,B、D的焰色反应均为黄色。C是一种酸式盐,将C加入BaCl2溶液有不溶于盐酸的白色沉淀生成,D晶体在干燥空气中容易逐渐失去结晶水变成白色粉末。对A、B、C、D进行下列实验,实验过程和记录如下图所示(无关物质已略去),请回答:
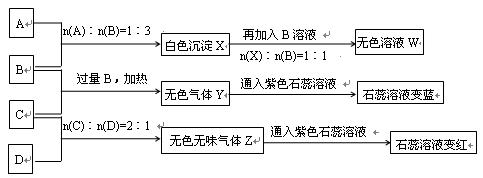
(1)X与B反应的离子方程式为 。
(2)D溶液pH值大于7,原因是(用离子方程式表示) 。
(3)写出C与过量B反应(加热)的离子方程式 __________________ 。
(4)若B、C的稀溶液混合后(不加热)溶液呈中性,则该溶液中离子浓度从大到小的顺序_____________________.
(5)Y在同主族的同类物质中分子稳定性最强( ),也是沸点最高的( )。(判断正误填"是"或"否")
(6)若向三份足量的B的稀溶液中分别加入少量稀醋酸、稀硝酸、浓硫酸,均生成1molH2O时的反应热分别为△H1 ,△H2,△H3 ,则三者由大到小排序为:___________________.
答案
(1) Al(OH)3+OH— = AlO2— +2H2O(2分)
(2)CO32—+ H2O  HCO3—+OH— (2分)
HCO3—+OH— (2分)
(3)NH4+ +H+ +2OH—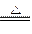 NH3↑+2H2O(3分)
NH3↑+2H2O(3分)
(4)C(Na+)>C(SO42-)>C(NH4+ )>C(H+) = C(OH-) (3分)
(5)是 ,否 (各1分) (6)△H1 >△H2 >△H3 (2分)
