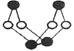
(14分)已知A、E、I、L是常见的非金属单质,其中A为淡黄色固体;Z是常见的金属单质,B的相对分子质量比A大32,C的相对分子质量比B大16,Y是一种常见的液体,J是磁性氧化铁, D、H、K均是重要的化工产品;X分子的球棍模型如图所示,组成X的两种元素的相对原子质量相差18。下列框图中部分反应条件已略去。
试回答下列问题: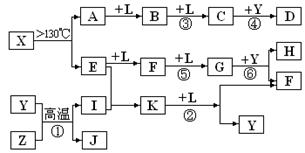
(1)下列有关X的说法正确的是 .
A.该物质的分子式为S4N4
B.该物质的分子中既有极性键又有非极性键
C.该物质具有很高的熔、沸点
D.该物质与化合物S2N2互为同素异形体
(2)E的电子式为 ,D的分子式 ,在反应①、②、③、④、⑤、⑥中属于非氧化还原反应的是 。(填序号)
(3)写出反应②的化学方程式: 。
(4)J与过量H的稀溶液反应的离子方程式为 。
1)AB(2分)(2)N2电子式略,H2SO4,④(各2分)
(3)4NH3 + 5O2  4NO +6 H2O(3分)
4NO +6 H2O(3分)
(4)3Fe3O4 + 28H+ + NO3- = 9Fe3+ + NO↑+ 14H2O(3分)
