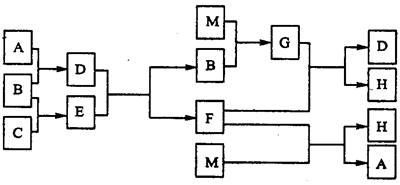
在元素周期表短周期元素中,A、B、C、M是单质。M是一种日常常用金属,有关转化如图:
请回答:
(1)元素M在元素周期表的位置: 周期, 主族。
(2)①写出B与C在加热条件下反应的化学方程式:
② C与D反应的化学方程式为:
③写出M与F的水溶液反应的离子方程式:
(3)将1mol E和1mol碳酸氢钠混合放在密闭容器中加热,加热至300℃经充分反应后排出气体。
写出:
①容器内残留的固体物质名称及其物质的量 ;
②在容器中发生的化学反应的化学方程式: ;
(15分)
(1)三,ⅢA(各1分)
(2)2Na+O2 Na2O2(2分) 2Na+2H2O=2NaOH+H2↑(2分)
(3)2Al+2OH—+2H2O 2AlO2—+3H2↑(2分)
(4)碳酸钠(1分),1mol(1分),氢氧化钠(1分) 1mol(1分)
2NaHCO3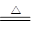 Na2CO3+H2O↑+CO2↑ 2Na2O2+2CO2
Na2CO3+H2O↑+CO2↑ 2Na2O2+2CO2 2Na2CO3+O2
2Na2O2+2H2O===4NaOH+O2(每个1分)
一定要注意本题所涉及的元素均为短周期元素,M是一种日常常用金属,可知M为铝。铝和单质B可反应,根据B的化合物及性质,可猜测B为氧气;进而可知D、E分别是由A、C和氧气反应得到,均为氧化物且可反应产生氧气,可推测出D、E应该是Na2O2、CO2或Na2O2、H2O;再由D、E的产物F可与铝反应可知D、E应该是Na2O2、H2O反应生成了F:NaOH。由F(NaOH)与M(铝)反应生成了A与H,可知A为氢气。
到此为止,可知A、B、C分别为氢气、氧气、钠单质。
(3)将1mol Na2O2和1mol碳酸氢钠混合放在密闭容器中加热,发生下列反应:
2NaHCO3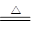 Na2CO3+H2O↑+CO2↑
Na2CO3+H2O↑+CO2↑
2Na2O2+2CO2 2Na2CO3+O2
2Na2O2+2H2O===4NaOH+O2(每个1分)
NaHCO3分解产生的两个气体恰好与Na2O2反应生成相应的产物。
