(每空2分,共14分)A、B、C、D、E、F六种中学化学中常见的物质,有如图转化关系,则:

(1)若A、C、E皆为氧化物,且E为有毒气体,B、D、F皆为非金属单质,且D为气体。则A的结构简式为 ,单质F的晶体类型为 ,1molC中含有 个共价键。
(2)若A、C、E皆为氢化物,三者皆为极性分子,其中C的相对分子质量最小;D、E、F皆为氧化物,其中D、F为有毒气体,F遇空气变为红棕色则。
①A、C、E沸点由高到低的顺序为 ,(填化学式);A、C、E三种气态氢化物稳定性最强的是 (填化学式)。
②B跟C反应生成E和F的化学方程式为 。
③A跟D常温下反应可生成一种单质,化学方程式为 。
(每空2分,共14分)(1)H-O-H,原子晶体,4NA;(2)①H2O>NH3>H2S,H2O;
②4NH3 + 5O2 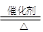 4NO +6 H2O, ③SO2 + 2H2S=2H2O + 3S↓
4NO +6 H2O, ③SO2 + 2H2S=2H2O + 3S↓
(1)根据题意反应都是置换反应,由于E为有毒气体,所以E水CO,则A是水,B是碳,C是二氧化硅,D是氧气,F是硅。在二氧化硅晶体,每个硅原子形成4个硅氧键,所以1mol二氧化硅中含有4NA个共价键。
(2)D、F为有毒气体,F遇空气变为红棕色,则F是NO,C是氨气,B是氧气,E是水,A是硫化氢,D是SO2。
①水分子间、氨气分子间都存在氢键所以沸点都高于硫化氢的,即H2O>NH3>H2S。非金属性越强,氢化物的稳定性越强,水最稳定。
②该反应是氨的催化氧化,方程式为4NH3 + 5O2 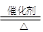 4NO +6 H2O。
4NO +6 H2O。
③SO2具有氧化性,能和氧化硫化氢生成单质硫和水,方程式为SO2 + 2H2S=2H2O + 3S↓。
