(12分)根据下列框图关系填空。已知反应①、③是工业生产中的重要反应,D、E常温下为气体、X常温下为五色液体,H与E相对分子质量之间的关系为:Mr(H)-Mr(E)=34,又知C的焰色反应呈黄色。

(1)化合物B中所包含的化学键有___________________
(2)反应④的离子方程式:________________________________
反应⑤的化学方程式:________________________________
(3)已知每生成16gE,放出106.5kJ热量,则反应①的热化学方程式为:
______________________________________ (1)离子键、非极性键(或共价键)
(2)Fe203+6H+=2Fe3++3H20, Fe2(S04)3+6NaOH =2Fe(OH)3↓+3Na2S04
(3)FeS2(s)+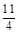 02=
02=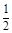 Fe2O3 (s) +2SO2(g);△H=-852kJ/mol
Fe2O3 (s) +2SO2(g);△H=-852kJ/mol
(未注明状态扣1分,写成FeS给2分)
本题是无机框图题,根据是找准突破点。C的焰色反应呈黄色,说明含有钠元素。X是液体,所以X是水。反应①、③是工业生产中的重要反应,因此可能是工业制取硫酸的,即A是FeS2,D是氧气,F是氧化铁,E是SO2。所以B是过氧化钠,C是氢氧化钠,G是三氧化硫,H是硫酸,则I是硫酸铁,J是氢氧化铁。
