(10分)置换反应的通式可表示为(转化中涉及的均为中学化学的常见物质):
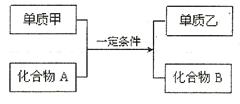
请回答下列问题:
(1)若单质甲与化合物A发生的反应常用于野外焊接钢轨,则该反应的化学方程式为 ;
(2)若甲、乙分别是同主族的两种非金属固体单质,则化合物A的一种主要用途是 ;
(3)若甲、乙分别是同主族短周期元素的两种单质,化合物B是一种强碱,则反应的离子方程式为 ;
(4)若组成单质乙的元素的最外层电子数是次外层电子数的2倍,金属单质甲能在化合物A中燃烧,则该反应中氧化剂与还原剂的物质的量之比为 ;若反应中生成2.4g单质乙,则消耗的化合物A在标准状况下的体积为 。
(共10分)(1)2Al+Fe2O3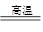 Al2O3+2Fe(2分) (2)作光导纤维(2分)
Al2O3+2Fe(2分) (2)作光导纤维(2分)
(3)2Na+2H2O=2Na++2OH-+H2↑(2分) (4)1:2(2分) 4.48L(2分)
(1)若单质甲与化合物A发生的反应常用于野外焊接钢轨,则反应一定是铝热反应,方程式是2Al+Fe2O3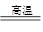 Al2O3+2Fe。
Al2O3+2Fe。
(2)若甲、乙分别是同主族的两种非金属固体单质,则甲和乙分别是碳和硅,则A是二氧化硅,B是CO。二氧化硅的主要用途之一是作光导纤维。
(3)若甲、乙分别是同主族短周期元素的两种单质,化合物B是一种强碱,则B是氢氧化钠,A是水,甲是钠。乙是氢气,反应的方程式是2Na+2H2O=2Na++2OH-+H2↑。
(4)元素的最外层电子数是次外层电子数的2倍,则乙是碳。金属单质甲能在化合物A中燃烧,所以A是CO2,甲是镁,B是氧化镁,乙是碳。工业的方程式水解2Mg+CO2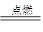 2MgO+C,其中CO2是氧化剂,镁是还原剂,二者的物质的量之比是1:2。2.4碳是0.2mol,所以需要CO2是0.2mol,标准状况下的条件是4.48L。
2MgO+C,其中CO2是氧化剂,镁是还原剂,二者的物质的量之比是1:2。2.4碳是0.2mol,所以需要CO2是0.2mol,标准状况下的条件是4.48L。
