(16分)以下是有关物质相互转化的关系图,其中A俗称铁红,甲为强酸,乙为还原性气体,丙为强碱溶液,G为红褐色沉淀,I的颜色呈浅绿色。
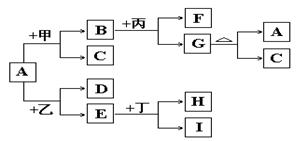
(1)若F是由Na+和SO42-组成的溶液,则甲的化学式是 ,列举A物质的一种用途 。
(2)若D是能使澄清石灰水变浑浊的气体,则乙的化学式为 ,丁属于单质、酸、碱中的 ;在I溶液中加入氢氧化钠溶液,可以观察到的现象是 ,对应的离子方程式和化学方程式依次是 ,
;
(3)写出G A+C的化学方程式: 。
A+C的化学方程式: 。
(4)若A中混有杂质Al2O3,除去杂质的方法是加入过量的 ,该反应的离子方程式为 。
(5)由E和A组成的混合物与稀H2SO4作用,固体恰好溶解,所得溶液中不含Fe3+,且生成的Fe2+与H2的物质的量之比为4:1。则反应物中Fe2O3、Fe、H2SO4的物质的量之比为____ ____。
(16分)(1)H2SO4,用做红色油漆和涂料
(2)CO, 酸;
生成白色沉淀,迅速变为灰绿色,最终变为红褐色,
Fe2++2OH-=Fe(OH)2↓,4Fe(OH)2+O2+2H2O="4" Fe(OH)3;
(3)2Fe(OH)3 Fe2O3+3H2O
Fe2O3+3H2O
(4)NaOH溶液,Al2O3+2OH-=2AlO2-+H2O
(5)1: 2:4(3分)
题目分析:A俗称铁红,则是三氧化二铁,G为红褐色沉淀,则是氢氧化铁,I的颜色呈浅绿色,含有亚铁离子。
(1)由F为硫酸钠、G为红褐色氢氧化铁沉淀,根据复分解反应的特点,可推测B、丙分别为硫酸铁和氢氧化钠;结合B为氧化铁与甲反应生成物,可判断甲为硫酸,C为水;
(2)由D是能使澄清石灰水变浑浊的气体,可判断气体D为二氧化碳;而反应A+乙→D+E中物质A为氧化铁,乙为还原性气体,则为CO,E为单质铁;再由I的溶液呈浅绿色,可推断I为亚铁离子,丁为一种酸,可能是盐酸或硫酸等,不能是氧化性的硝酸。亚铁与碱反应生成白色沉淀,迅速变为灰绿色,最终变为红褐色,方程式为Fe2++2OH-=Fe(OH)2↓,4Fe(OH)2+O2+2H2O="4" Fe(OH)3;
(3)氢氧化铁在加热条件下会分解为氧化铁与水:2Fe(OH)3 Fe2O3+3H2O
Fe2O3+3H2O
(4)除去氧化铁中氧化铝一般是加入氢氧化钠溶液,碱只与两性氧化物氧化铝反应;
(5)假设H2为1mol,则Fe2+为4mol;
根据方程式
Fe+H2SO4=FeSO4+H2;
1mol 1mol 1mol 1mol
上述反应中生成Fe2+为1mol,则还有3mol Fe2+由铁与三价铁生成:
Fe 2(SO4)3+ Fe= 3FeSO4
1mol 1mol 3mol
可知Fe 2(SO4)3为1mol,Fe为2mol。
Fe2O3+3H2SO4=Fe 2(SO4)3+3H2O;
1mol 3mol
则硫酸一共是4mol,所以比例是1: 2:4
点评:铁三角的转化及计算是高中的一个难点,本题综合考查了铁三角知识,同时在转化中涉及到计算,属于较难的一道综合题。
