已知A、B、C、D是中学化学中常见的四种不同粒子,它们之间存在如图所示的转化关系(反应条件已经略去):
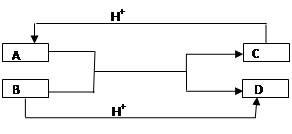
(1) 如果A、B、C、D均是10电子的粒子,请写出A、D的化学式:
A____________ D_______________
(2)如果A和C是18电子的粒子,B和D是10电子的粒子,请写出:
① A与B在溶液中反应的离子方程式为:___________________________________
② 根据上述离子方程式,可以判断C与B结合质子的能力大小是(用化学式或离子符号表示)_________________________________________________。
(1)A :NH4+ D :H2O
(2)① HS-+OH-=S2-+H2O (或H2S+2OH-=S2-+2H2O)
② OH->HS- (或OH- >S2-)
题目分析:(1)如果A、B、C、D均是10电子的粒子,结合10电子微粒进行分析判断;10电子微粒:
一核:Ne、N3-、O2-、F-、Na+、Mg2+、Al3+ ;二核:HF、OH-;三核:H2O、NH2-;四核:NH3、H3O+ ;
五核:CH4、NH4+。根据发生反应A+B=C+D,A、B、C、D均是10电子的粒子,可判断为:A、B分别为OH-、NH4+,C、D分别为NH3、H2O。又因为B和氢离子反应生成D,所以B是OH-,D是水,A是NH4+,C是氨气。氨气和氢离子反应生成NH4+。
(2)如果A和C是18电子的粒子,B和D是10电子的粒子,则根据反应式A+B=C+D可知,符合条件是HS-+OH-=S2-+H2O或H2S+2OH-=S2-+2H2O。又因为B和氢离子反应生成D,所以B是OH-,D是水,A是HS-或H2S,C是S2-。
① A与B在溶液中反应的离子方程式为HS-+OH-=S2-+H2O (或H2S+2OH-=S2-+2H2O)
②根据方程式HS-+OH-=S2-+H2O (或H2S+2OH-=S2-+2H2O)可知,C与B结合质子的能力大小是OH->HS- (或OH->S2-)。
点评:该题综合性强,对学生的思维能力要求高,有利于培养学生的逻辑思维能力和发散思维能力。本题主要是考查原子核外电子结构特征,物质转化关系的应用,主要是10电子和18电子微粒的分析和应用。熟练掌握常见10电子和18电子微粒是解题关键。
