在下图所示的物质转化关系中,A是海水中含量最丰富的盐,B是常见的无色液体,F在D中燃烧发出苍白色火焰。H可用于制造光导纤维,J是一种乳白色凝胶状沉淀。(部分生成物和部分反应条件未列出)
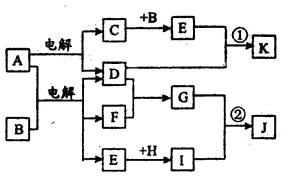
请回答下列问题:
(1)A的电子式为
形成单质D的元素在周期表中的位置
(2)形成C、D、F单质的元素半径由大到小的顺序(填写元素符号)
(3)C长期暴露在空气中,最终产物是
(4)H的化学式为 H在高温下与碳反应,若转移4mol电子参加反应的碳为 mol。
(5)写出反应①的离子方程式
(6)写出反应②的化学方程式
(1) (1分)3 ⅦA(1分)
(1分)3 ⅦA(1分)
(2)Na >Cl>H(2分)
(3)Na2CO3(2分)
(4)SiO2(2分)2(2分)
(5)Cl2+2OH―=Cl―+ClO―+H2O(2分)
(6)Na2SiO3+2HCl=H2SiO3↓+2NaCl(2分)
A是海水中含量最丰富的盐,A是NaCl,B是常见的无色液体,B为水,F在D中燃烧发出苍白色火焰,F为H2,D是Cl2。H可用于制造光导纤维,H为SiO2,J是一种乳白色凝胶状沉淀。J是H2SiO3;结合图:C是Na; E是NaOH,G 是HCl,I是Na2SiO3.
(1)A是NaCl,A的电子式为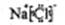 ,D是Cl,在第三周期,ⅦA族;答案:
,D是Cl,在第三周期,ⅦA族;答案: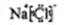 、3 ⅦA
、3 ⅦA
(2)C、D、F单质分别是Na、Cl、H ,Na、Cl位于同一周期,从左到右原子半径变小,Na >Cl,H 是原子半径最小的原子;答案:Na >Cl>H
(3)Na在空气中,先后变化成Na2O、NaOH溶液、Na2CO3溶液、Na2CO3·10H2O,最终变成Na2CO3,答案:Na2CO3;
(4)H的化学式为SiO2,2C+SiO2 2CO+Si,由方程式,每有2molC反应转移电子4mol,答案:SiO2 2
2CO+Si,由方程式,每有2molC反应转移电子4mol,答案:SiO2 2
(5)反应①的离子方程式Cl2+2OH―=Cl―+ClO―+H2O,答案:Cl2+2OH―=Cl―+ClO―+H2O
(6)反应②的化学方程式Na2SiO3+2HCl=H2SiO3↓+2NaCl,答案:Na2SiO3+2HCl=H2SiO3↓+2NaCl。
