学习常见金属的化学性质和金属的活动性顺序,能帮助我们发现和研究更多的金属.
(1)根据下图回答有关问题:
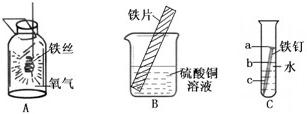
①写出实验A中反应的主要实验现象______.
②实验B中可观察到铁片的表面______现象,说明铁的金属活动性比铜______.(填“强”或“弱”)
③实验C中可观察到试管中铁钉最先生锈的是______处.(填“a”或“b”或“c”)
(2)所谓合金,就是不同种金属(或金属与非金属)在熔化状态下形成的一种熔合物.
| Na | Cu | Al | Fe | |
| 熔点(℃) | 97.5 | 1083 | 660 | 1535 |
| 沸点(℃) | 883 | 2595 | 2200 | 3000 |
a.Cu和Al b.Fe和Cu c.Fe和Na
(3)某兴趣小组的同学在实验室为了比较银白色金属R与铁的活动性强弱,设计了下列方案进行实验,请你帮他们完成下表______:
| 你的一种猜想 | 验证方法 | 现象 | 结论 |
| 金属R的活动性比铁 _______ | 将金属R投入 _______溶液中 | 金属R表面有黑色的物质析出 | 猜想 _______ (选填“正确”或“错误”) |
(1)①图示为铁丝在氧气中燃烧,可观察到:剧烈燃烧,火星四射,放热,生成黑色固体(答出火星四射即可给分);
故答:剧烈燃烧,火星四射,放热,生成黑色固体;
②铁片放入蓝色硫酸铜溶液,铜被置换出来,所以会看到铁片表面有红色物质;此实验验证了铁的活动性比铜强;
故答:铁片表面覆盖一层红色物质,强;
③铁在与氧气、水同时接触时生锈,图中所示实验b处既接触水又接触氧气,所以最先被锈蚀;
故选B;
(2)合金是不同种金属在熔化状态下形成的一种熔合物,即两种金属都成为液态时进行混合;
由于金属钠的沸点较低,在铁熔化时温度达1535℃,而此时金属钠已变成气态,无法完成液态时混合;
故选C;
(3)所设计探究实验是比较银白色金属R与铁的活动性强弱的实验,根据实验中的现象“有黑色物质析出”可推断:把金属R放入亚铁盐溶液中,通过置换出铁的实验现象,得到R的活动性比铁强的结论.所以在回答时,要注意猜想与结论的一致性;
故答:强,FeSO4(或FeCl2等),正确(或:弱,FeSO4(或FeCl2等),错误).
