问题
问答题
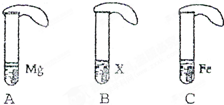
在相同条件下,金属与酸发生反应的速率越快,金属的活动性就越强.为了探究金属Mg、Fe和某金属X等三种金属的活动性顺序,研究性学习小组设计了如下实验(如图).
(1)取A、B、C三支相同的试管,分别加入足量的表面积相等的Mg、X、Fe各一片.
(2)再分别同时加入2mL浓度相同的盐酸溶液,立即把三个相同的气球分别套紧在各试管口上.实验现象如表:
| 编号 | A | B | C |
| 现象 | 金属表面有大量气泡冒出,气球膨胀速度快 | 金属表现无气泡冒出,气球不膨胀 | 金属表面有气泡冒出,气球膨胀速度较慢 |
②实验结果表明Mg、X、Fe三种金属的活动性由强到弱的顺序是______.
③实验中铁与稀盐酸反应的化学方程式:______.
④生活中哪种现象能证明铁比铜金属性活泼:______.
答案
①B中试管没有产生气体,可以判断该物质不能和酸反应,所以该金属是一种排在氢后的金属,如银等金属;
②金属与酸反应时反应越剧烈,金属的活动性越强,所以这三种金属的活动性顺序为:Mg、Fe、X;
③铁与盐酸反应生成了氯化亚铁和氢气,可以据此写出该反应的化学方程式为:Fe+2HCl═FeCl2+H2↑;
④根据铁在潮湿的空气中更容易生锈,所以可判断铁的活动性比铜的强.
故答案为:①后;银;
②Mg、Fe、X;
③Fe+2HCl═FeCl2+H2↑;
④铁在潮湿的空气中更容易生锈.
