问题
选择题
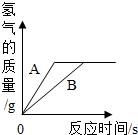
某研究性学习小组的同学为探究实验室制取氢气的方案,分别用等质量的金属A,B跟质量相同、溶质质量分数相同的稀硫酸反应,反应生成氢气的质量与时间的关系如下图所示.分析图象得到的下列结论中,不合理的是(已知A,B在生成物中均显+2价,A,B的相对原子质量不等)( )
A.反应速率A>B
B.生成氢气的质量A=B
C.金属的活动性A<B
D.金属足量,酸完全反应
答案
A、由图象可知等时间内金属A比金属B生成的氢气多,所以反应速率A>B.故A合理.
B、由图象可知最终金属A和金属B生成的氢气质量相等.故B合理.
C、金属的活动性越强,反应越快,所以金属的活动性:A>B.故C不合理.
D、因为A,B在生成物中均显+2价,A,B的相对原子质量不等,结合化学方程式可知,要生成等质量的氢气,需要的酸质量必须相等,而且反应掉金属的质量不能相等,所以酸完全反应,金属应该足量.故D合理.
故选C.
