问题
计算题
有A、B、C、D四种短周期元素。已知一个B原子核的原子受到α粒子的轰击得到一个A原子的原子核和一个C原子的原子核,又知C、D元素同主族,且能发生下面两个反应,如下图:
A、B化合物+B、C化合物 B单质+A、C化合物
B单质+A、C化合物
A、D化合物+D、C化合物 D单质+A、C化合物
D单质+A、C化合物
请完成下列问题。
(1)比较B、C原子半径大小;画出D离子的结构示意图。
(2)分别写出上述两个反应方程式。
答案
(1)B>C 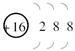 (2)2NH3+N2O3====2N2+3H2O 2H2S+SO2====3S↓+2H2O
(2)2NH3+N2O3====2N2+3H2O 2H2S+SO2====3S↓+2H2O
此题给出的条件较多,也较隐晦,我们要善于从中找出突破口。α粒子即氦核,这句话其实是告诉我们B与A和C在原子序数上的关系,即A与C的原子序数的和等于B的原子序数加上2。从给出的两个反应中我们看出,这两个反应都是氧化还原反应中的归中反应。B、D都为具有可变价态的非金属元素,再结合C与D同族,两个反应物的物质的量之比为2∶1等条件,不难判断,在短周期中这样的例子是2H2S+SO2====3S↓+2H2O。这样,A为氢,C为氧,D为硫就可定下来了。结合前面原子序数的关系,可判断出B为氮。那么第
一个反应就是NH3与NxOy生成N2和H2O的反应。至于是哪一种氮的氧化物,根据电子得失守恒则可计算出是N2O3。
