问题
填空题
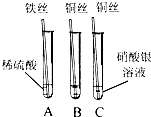
某同学在实验室完成了如右图所示的实验试管A中的现象是______,试管C中反应的化学方程式是______,B试管中的溶液是______,可以得出三种金属的活动性由强到弱的顺序是______.
答案
铁排在顺序表中氢的前面,因此可与酸反应生成氢气,,所以可观察到气泡生成,铜排在银的前面,所以铜和硝酸银可反应生成银和硝酸铜,方程式是Cu+2AgNO3═Cu(NO3)2 +2Ag,由A、C可知铁排在氢前,Cu>Ag,但是铁和铜的活动性强弱还无法判断,所以可在B中放入稀硫酸或稀盐酸,观察无气泡产生,说明铜在氢后,说明,或者在B中放入可溶性亚铁盐,如氯化亚铁,铜表面无现象,说明Fe>Cu,从而得出三种金属的活动性顺序;
故答案为:
有气泡产生;Cu+2AgNO3═Cu(NO3)2 +2Ag;稀硫酸(或其他可溶性亚铁盐或稀盐酸);铁、铜、银.
