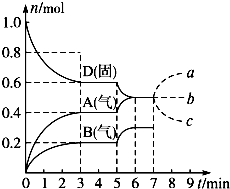
在容积为2.0L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,据图回答下列问题:
(1)从反应开始到第一次达到平衡时,A物质的平均反应速率为______mol•(L•min)-1.
(2)根据上图写出该反应的化学方程式______,该反应的平衡常数表达式为K=______.
(3)第5min时,升高温度,A、B、D的物质的量变化如上图,则该反应的正反应是______(填“放热”或“吸热”)反应,反应的平衡常数______(填“增大”“减小”或“不变”,下同),B的反应速率______.
(4)若在第7min时增加D的物质的量,A的物质的量变化正确的是______(用图中a、b、c的编号回答).
(5)一定温度下,在1L密闭容器中充入1molN2和3molH2并发生反应.若容器容积恒定,10min达到平衡时,气体的总压强为原来的
,则N2的转化率α(N2)=______.9 10
(1)从反应开始到第一次达到平衡时,A物质的平均反应速率为
=0.067mol/L•min,0.4mol 2.0L 3min
故答案为:0.067;
(2)根据图象知,随着反应的进行,D的物质的量减少,A、B的物质的量增加,所以D是反应物,A、B是生成物;同一反应、同一时间段内,各物质的浓度变化量之比等于其计量数之比,0-3min时,△D=0.4mol,
△A=0.4mol,△B=0.2mol,△D:△A:△B=0.4mol:0.4mol:0.2mol=4:4:2,方程式为:2D(s)⇌2A(g)+B(g);
故答案为:2D(s)⇌2A(g)+B(g)
因D为固体,所以化学平衡常数K=C2(A)×C(B),
故答案为:K=C2(A)×C(B);
(3)温度升高,D的物质的量减少,A、B的物质的量增大,平衡正向移动,而温度升高,平衡向吸热的方向移动,说明正反应为吸热反应,
平衡常数只有与温度有关,温度升高,平衡正向移动,平衡常数增大;
温度升高化学反应B的反应速率加快;
故答案为:吸热;增大;增大;
(4)D为固体,增加D的物质的量,浓度不变,平衡不移动,故选:b;
(5)一定温度下,在1L密闭容器中充入1molN2和3molH2并发生反应.若容器容积恒定,10min达到平衡时,气体的总压强为原来的
,依据化学平衡三段式列式计算,设氮气消耗物质的量为x;9 10
N2+3H2=2NH3
起始量(mol) 1 3 0
变化量(mol) x 3x 2x
平衡量(mol) 1-x 3-3x 2x
气体的总压强为原来的
,则1-x+3-3x+2x=9 10
×(1+3)9 10
x=0.2mol
则N2的转化率α(N2)=
×100%=20%;0.2mol 1mol
故答案为:20%.
