液氨常用作制冷剂,回答下列问题
(1)一定条件下在密闭容器中发生反应:
a.NH4I(s)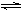 NH3(g) + HI(g) b.2HI(g)
NH3(g) + HI(g) b.2HI(g) 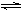 H2(g) + I2(g)
H2(g) + I2(g)
①写出反应a的平衡常数表达式
②达到平衡后,扩大容器体积,反应b的移动方向 (填“正向”、“逆向”或“不移动”),达到新的平衡时容器内颜色将怎样变化 (填“加深”、“变浅”或“不变”)
(2)工业上合成氨的反应:N2(g)+3H2(g) 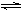 2NH3(g) ΔH=-92.60 kJ·mol-1
2NH3(g) ΔH=-92.60 kJ·mol-1
下列说法能说明上述反应向正反应方向进行的是________(填序号)。
a.单位时间内生成2n mol NH3的同时生成3n mol H2
b.单位时间内生成6n mol N—H键的同时生成2n mol H—H键
c.用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1∶3∶2
d.混合气体的平均摩尔质量增大
e.容器内的气体密度不变
(3)已知合成氨反应在某温度下2 L的密闭容器中进行,测得如下数据:
| 时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | 1.00 | 1.00 |
根据表中数据计算:
①反应进行到2 h时放出的热量为________ kJ。
②0~1 h内N2的平均反应速率为________ mol·L-1·h-1。
③此温度下该反应的化学平衡常数K=________(保留两位小数)。
④反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1.00 mol,化学平衡将向________方向移动(填“正反应”或“逆反应”)。
(4)肼(N2H4)的性质类似于NH3,极易溶于水,与水反应生成一种二元弱碱在溶液中分步电离,请用离子反应方程式表示其水溶液显碱性的原因
(1)① k=[NH3] [HI] ② 正向 变浅(2) bd
(3)①27.78 ②0.05 ③0.15 ④正反应
(4)N2H4·2H2O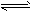 [N2H5·H2O]+ + OH-
[N2H5·H2O]+ + OH-
题目分析:(1)①根据题给反应a结合平衡常数表达式的书写原则写出,反应a的平衡常数表达式为k=[NH3] [HI];②反应a是反应前后气体体积增大的反应,反应b是反应前后气体体积不变,所以增大容器体积相当于压强减小,平衡向气体体积增大的方向移动,所以平衡向正反应方向移动,因为容器体积增大,平衡时I2(g)的浓度减小,气体颜色变浅;(2)a.单位时间内生成2nmolNH3的同时消耗3nmolH2,同时生成3n molH2,该反应达到平衡状态,错误;b.当单位时间内生成6nmolN-H键同时消耗3nmolH-H键反应处于平衡状态,现同时生成2n molH-H键,则平衡向在反应方向移动,正确;c.反应处于任何状态,用N2、H2、NH3的物质的量浓度变化表示的反应速率之比均等于化学计量数之比,为1:3:2,不能确定该反应向正反应方向移动,错误;d.混合气体的平均摩尔质量增大,则平衡向气体体积减小的正反应方向移动,正确;e.混合气体质量不变,容器体积不变,所以容器内的气体密度始终不变,错误;选:bd;(3)①根据题给数据分析,反应进行到2 h时生成氨气0.6mol,结合题给热化学方程式计算放出的热量为27.78 kJ;②根据题给数据分析,0~1 h内N2的物质的量变化为0.1mol,根据公式v=Δn/VΔt计算,平均反应速率为0.05 mol·L-1·h-1;③根据题给数据分析,反应达到平衡后c(NH3)=0.5mol/L,c(N2)=0.5mol/L,c(H2)=1.5mol/L,化学平衡常数K=[NH3]2/[N2][H2]3=0.15;④反应达到平衡后,再加入N2、H2和NH3各1.00 mol,c(NH3)=1mol/L,c(N2)=1mol/L,c(H2)=2mol/L,浓度商Q=0.125<K,则平衡向正反应方向移动;(4)肼(N2H4)的性质类似于NH3,极易溶于水,与水反应生成一种二元弱碱N2H4•2H2O,电离方程式为:N2H4•2H2O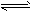 [N2H5•H2O]++OH-。
[N2H5•H2O]++OH-。