问题
问答题
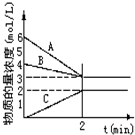
已知N2+3H2⇌2NH3,根据如图判断:
A是______的物质的量浓度变化情况.反应开始时,C(N2)=______;
2min时C(NH3)=______,0-2min内氢气的平均反应速率v(H2)=______.
答案
随反应进行反应物的物质的量减小,生成物的物质的量增大,因此AB为反应物,C为生成物,反应消耗的物质的量之比等于化学计量数之比,图中变化量最大的为氢气;所以A为H2,B为N2,C为NH3;由图象可知反应开始时,C(N2)=4mol/L;2min时C(NH3)=2mol/L;
0-2min内氢气变化的浓度为△c(H2)=6-3mol/L=3mol/L,所以0-2min内氢气的平均反应速率v(H2)=
=△c(H2) t
=1.5mol/(L•min);3mol/L 2min
故答案为:H2;4mol/L;2mol/L;1.5mol/(L•min).
