A、B、C、D、E为五种短周期元素,其中A、B、C位于同一周期,A元素的气态氢化物是一种广泛应用的优质气体燃料,B元素的氢化物是用途最为广泛的溶剂。B元素可分别与A、C、D、E组成RB2型化合物。已知在DB2中,D与B的质量比为7 :8;在EB2中,E与B的质量比为1 :1。根据以上条件回答下列问题:
(1)请写出C单质分子的电子式______________;DB2晶体中化学键的类型为_____________;写出AE2的结构式 ___________________。
(2)C的气态氢化物易液化,原因是___________________。
(3)C和D结合可生成一种超硬物质,有关该物质性质的叙述中不正确的是______________________.
①有润滑性 ②易磨损 ③抗腐蚀 ④强还原性 ⑤抗冷热
(4)B元素可分别与A、E形成多种由两种元素构成的阴离子。某溶液是由其中若干种阴离子组成的无机钠盐溶液,为了检验该溶液中的阴离子,分别取两份溶液进行如下实验:
①第一份溶液中加入足量盐酸,只产生无色气体;
②第二份溶液中加入足量的BaCl2溶液,有白色沉淀产生,再缓慢加入足量的稀硝酸,白色沉淀质量减少。由此得出的结论是_______________________。
(5)E元素的一种氧化物可与过氧化钠及氯水发生氧化还原反应。该氧化物与过氧化钠反应的化学方程式为_______________________;该氧化物与氯水反应的离子方程式为____________________________。
(共15分)
(1)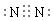 ;(2分)(极性)共价键;(1分) S=C=S。(2分)(共5分)
;(2分)(极性)共价键;(1分) S=C=S。(2分)(共5分)
(2) C的氢化物分子之间存在有氢键,使其沸点较高(2分)
(3) ②④ (2分)
(4) 一定有CO32—,SO32— 和SO42— 至少有一种
(若答S2O32—一定不存在亦对,不答此项亦可) (2分)
(5) SO2 + Na2O2 = Na2SO4 ; SO2 + Cl2 + 2H2O = 4H+ + SO42- + 2Cl-(4分,每空2分)
