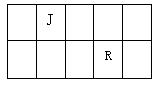
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最高正化合价与最低负化合价的绝对值相等;M是地壳中含量仅次于氧元素的非金属元素;L的最简单气态氢化物甲能使湿润的红色石蕊试纸变蓝。
(1)M的原子结构示意图为________ ;元素R在周期表中位于第_____周期,第_____族, 元素T最高价氧化物对应水化物化学式是________。
(2)写出J和氧形成的一种酸性氧化物的电子式____________,含有共价键是______(填极性键或非极性键)。
(3)写出能说明T非金属性比R强的反应的化学方程式___________________________
(4)在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为______________________________________
(5)0.2mol由M形成的气态氢化物在O2中完全燃烧,生成一种固体和液态水,298K时放出热量a kJ 。 该反应的热化学方程式为_____________________________________________
(15分)(1)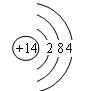 ;三、ⅥA;HClO 4
;三、ⅥA;HClO 4
(2)CO2电子式略,极性键
(3)Cl2+H2S=S+2HCl (或其他合理答案)
(4)2NH3·H2O+3H2O2=N2↑+8H2O或2NH3+3H2O2=N2↑+6H2O
(5)SiH4 (g)+2O2(g)=SiO2 (s)+2 H2O(l) ΔH=-5akJ/mol(方程式各3分,其他每空1分)
