问题
选择题
质量相等的镁、铝、铁三种金属分别与足量的盐酸反应,制取的氢气质量(y)和所用去的金属质量(x)之间的关系如下图所示,正确的是( )
A.

B.
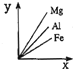
C.

D.

答案
质量相等的镁、铝、铁三种金属分别与足量的盐酸反应,则金属完全参加反应
设金属元素在化合物中的化合价为x,其相对原子质量为y,该金属为M,金属的质量为1g,生成氢气的质量为N,则有
2M+2xHCl═2MClx+xH2↑
2y 2x
1g N
=2y 1g 2x N
N=
gx y
则1g的Mg、Fe、Al生成氢气的质量分别为
g、2 24
g、2 56
g,由此可知等质量 的三种金属生成氢气的质量由多到少的顺序是铝、镁、铁;3 27
故选A.
