X、Y、Z为周期表中常见元素,原子序数递增,X、Y原子的最外层电子数是其电子层数的2倍,Z单质是生产生活中用量最大的金属。
(1)X、Y的原子可构成一种物质,该物质与某能引起温室效应的气体结构相同;该物质的电子式是 。
(2)下列含氧酸根离子的化学式书写不正确的是 (填序号)。
a.XO3- b.XO32- c.YO32- d.Y2O32- e. YO3- f. YO42-
(3)Z单质与其它化合物可满足如下转化关系:
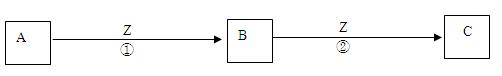
①C溶液在储存时应加入少量Z,其理由是(用文字和离子方程式回答)____ ____。
②将5~6滴B的饱和溶液滴入沸水中,可得到红褐色液体,该液体能产生丁达尔效应。该反应的离子方程式为 。
(4)Y的最高价含氧酸是重要的化工产品。
①已知YO2被空气氧化,每生成1mol气态YO3,放出98.3kJ热量。该反应的热化学方程式是 。
②实验测得相同条件下一定量的Y单质分别在空气和在氧气中充分燃烧后产物的成分(体积分数)如下表。
| YO2 | YO3 | |
| 空气 | 94%—95% | 5%—6% |
| 氧气 | 97%—98% | 2%—3% |
(1)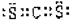 (1分) (2)a 、e(1分);
(1分) (2)a 、e(1分);
(3)①加入少量铁,防止Fe2+被氧化为Fe3+,2Fe3++Fe===3Fe2+ (1分)
②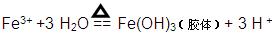 (1分)
(1分)
(4)①SO2(g)+1/2O2(g)="= " SO3(g) △H =" " — 98.3kJ·mol-1(1分)
②纯氧中O2的浓度大,反因应速率快,单位时间内放热多,体系温度高,平衡向SO3分解的方向移动,SO3含量低。(1分)
