我国的领海主权不容侵犯.南海是我国的固有领海,蕴藏着丰富的海洋资源.
(1)南海不仅蕴含着大量的煤、石油、天然气等常规化石燃料,还蕴藏着大量的可燃冰.可燃冰(主要成分是CH4)被科学家誉为“未来能源”,CH4燃烧的化学方程式是______.可燃冰作为能源与煤、石油相比的优点是______.
(2)南海某岛利用资源优势,建成海水综合利用基地,生产各种产品.
①从海水中获取淡水.目前能规模化和产业化淡化海水的方法主要是______.
②从海水中获得氯化钠.将海水进行______可得到粗盐.
③从海水中得到金属镁.用苦卤制取金属镁的流程图如下:
苦卤
氢氧化镁石灰乳 步骤Ⅰ
氯化镁稀盐酸 步骤Ⅱ
镁电解 步骤Ⅲ
苦卤本身含有MgCl2,又经历了步骤Ⅰ、Ⅱ的转化过程,其目的是______;无水MgCl2制取镁的化学方程式为______.
④以海水中获得食盐为原料制取纯碱.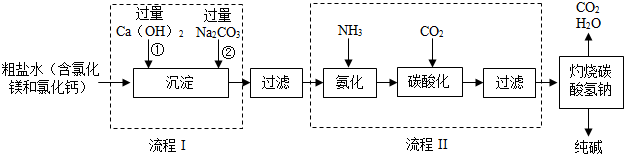
a.经过流程Ⅰ过滤后得到沉淀是______;(填物质的化学式)
b.流程Ⅱ中发生的总反应为______;
c.如果加入氨气不是为了产生氯化铵,那么,氨气在制碱过程中作用是______.
(1)天然气的主要成分甲烷燃烧的化学方程式为CH4+202
CO2+2H20;可燃冰作为能源与煤、石油相比的优点是同等条件下燃烧产生热量比煤和石油多,燃烧后几乎不产生任何残渣和废气;故答案为:CH4+202点燃 .
CO2+2H20 同等条件下燃烧产生热量比煤和石油多,燃烧后几乎不产生任何残渣和废气;点燃 .
(2)
①从海水中获取淡水.目前能规模化和产业化淡化海水的方法主要是膜法和热法;
②氯化钠的溶解度受温度影响变化不大,所以将高盐度浓缩海水进行蒸发结晶可以分离得到粗盐;故答案为:蒸发结晶;
③苦卤本身含有MgCl2,又经历了步骤Ⅰ、Ⅱ的转化过程,其目的是富集氯化镁,除去杂质获得比较纯净的氯化镁;无水MgCl2制取镁的化学方程式为MgCl2
Mg+Cl2↑;通电 .
④以海水中获得食盐为原料制取纯碱,粗盐水加入石灰乳是氯化镁和氢氧化钙反应生成氯化钙和氢氧化镁沉淀,氯化钙和碳酸钠反应生成氯化钠和碳酸钙沉淀,
故a、经过流程Ⅰ过滤后得到沉淀是Mg(OH)2 CaCO3;
b、流程Ⅱ中发生的总反应为NaCl+NH3+CO2+H2O=NH4Cl+NaHCO3;
c、氨气溶于水溶液呈碱性,故氨气在制碱过程中作用是使溶液显碱性,有利于二氧化碳的吸收;
答案:
(1)CH4+2O2
CO2+2H2O同等条件下燃烧产生热量比煤和石油多,燃烧后几乎不产生任何残渣和废气点燃 . .
(2)①膜法和热法
②蒸发结晶
③富集(或聚集)氯化镁,除去杂质获得比较纯净的氯化镁MgCl2
Mg+Cl2↑通电 . .
④a.Mg(OH)2CaCO3 b.NaCl+NH3+CO2+H2O=NH4Cl+NaHCO3↓c.使溶液显碱性,有利于二氧化碳的吸收
