将27g铝粉、56g铁粉分别与等质量、等质量分数的稀硫酸充分反应,生成氢气的质量与反应时间的关系如图.下列叙述与该曲线图相符的是( )
A.①表示铁粉与稀硫酸反应的情况
B.反应结束,铝、铁均完全反应,硫酸有剩余
C.反应结束,硫酸完全反应,铝、铁均有剩余
D.反应结束,硫酸、铁均完全反应,铝有剩余
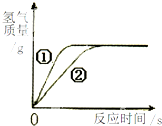
A.根据金属铝的活动性比铁强,则在相同时间内金属铝与稀硫酸反应放出氢气的速率大于铁;结合图示,可判断曲线①表示铝与硫酸的反应,曲线②表示铁与硫酸的反应;故A不正确;
B.根据铝、铁与稀硫酸反应的化学方程式可以知道:
2Al+3H2SO4 ═Al2(SO4)3+3H2↑
54 6
Fe+H2SO4 ═FeSO4+H2↑
56 2
根据27g铝粉完全反应可放出氢气的质量=
×27g=3g,而56g铁粉完全反应放出氢气的质量=6 54
×56g=2g;结合图示可知反应结束后所得氢气质量相等,因此可判断反应结束后两金属粉末一定不会均完全反应;故B不正确;2 56
C.若反应中稀硫酸质量不足完全反应而两金属都有剩余,根据B中反应的化学方程式分析可以知道所得氢气质量一定相等,这种情况与图示所示结果一致,故C正确;
D.由于27g铝粉完全反应可放出氢气的质量大于56g铁粉完全反应放出氢气的质量,所以,当铁粉与稀硫酸恰好完全反应时,因27g铝粉完全反应需要更多的稀硫酸而出现稀硫酸不足铝粉剩余,此时稀硫酸完全反应所产生氢气的质量也会相等;此时所出现的情况与图示结果一致,故D正确;
故选CD.
