问题
填空题
已知和碳元素同主族的X元素位于周期表中的第一长周期,短周期元素Y原子的最外层电子数比内层电子总数少3,它们所形成化合物的分子式是XY4。试回答:
(1)X元素的原子基态时电子排布式为 ;Y元素原子最外层电子的轨道表示式为 。
(2)若X、Y两元素电负性分别为1.8和3.0,则XY4中X与Y之间的化学键为 (填“共价键”或“离子键”)。
(3)该化合物的空间结构为 ,中心原子的杂化类型为 ,分子为 (填“极性分子”或“非极性分子”)。
(4)该化合物在常温下为液体,该化合物中分子间作用力是 。
(5)该化合物的沸点与SiCl4比较, (填化学式)的较高,原因是 。
答案
(1)1s22s22p63s23p63d104s24p2 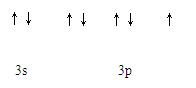
(2)共价键
(3)(3分)正四面体形 sp3杂化 非极性分子
(4)范德华力
(5)GeCl4 二者结构相似,GeCl4相对分子质量大,分子间作用力强,沸点高
