为测定一种气态烃A的化学式,取标准状况下一定体积的A置于密闭容器中,再通入一定体积的O2,用电火花引燃,定性实验表明产物是CO2、CO、水蒸气.相关方案及有关数据如下(图中的箭头表示气体的流向,试验前系统内的空气已排除),
试回答:(不要求写出计算过程)
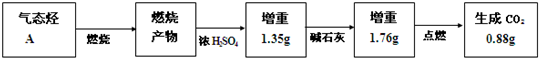
(1)燃烧后产物中水的物质的量______ mol
(2)燃烧后产物中二氧化碳的物质的量______ mol
(3)燃烧后产物中一氧化碳的物质的量______ mol
(4)通过计算求出A的实验式(最简式)______;
(5)根据所学知识,你认为气态烃A只能是哪种物质?你的根据是什么?A是______;根据是______.
(1)浓硫酸是吸水用的,所以水的质量是1.35g,物质的量为:
=0.075mol,故答案为:0.075;1.35mol 2
(2)碱石灰吸收了二氧化碳1.76g,物质的量为:
=0.04mol,故答案为:0.04;1.76g 44g/mol
(3)点燃一氧化碳后生成的二氧化碳0.88g,所以CO的物质的量=CO2的物质的量=
=0.02mol,故答案为:0.02;0.88g 44g/mol
(4)水中的H全部来自于A,所以A中的H原原子物质的量经过计算为0.15mol,点燃一氧化碳后生成的二氧化碳0.88g,所有二氧化碳总共2.64g,其中的C也全部来自于A,所以经过计算C是0.06mol,所以A中H与C的比例是5:2,最简式为:C2H5,故答案为:C2H5;
(5)A可能是C2H5,C4H10,C6H15…,因为A是气体,所以碳个数不超过4,另外当A饱和时,氢原子数等于碳原子数的2倍加2,所以很明显C2H5和C6H15这种物质是不存在的,所以A只能是
C4H10,故答案为:C4H10;①气态烃中的碳原子数≤4②烃中的氢原子数最多为碳原子数的2倍多2.
