问题
填空题
(11分)下表为元素周期表的一部分,a、b、c…为部分元素。回答下列问题:
| a | |||||||||||||||||
| f | y | h | i | ||||||||||||||
| b | e | j | |||||||||||||||
| c | d | [ | d | g | l | ||||||||||||
| [ | |||||||||||||||||
(2)ya3分子的电子式是 ,其分子的空间构型是 ,分子中y原子的杂化轨道类型是 , g2+可以与ya3以 键形成 [g (ya3)4]2+离子;
(3)请写出上述元素d3+的核外电子排布式 ,实验室常用形成一种红色配离子的方法检验该离子,该反应的离子方程式为
。
(4)请比较b、e、j三种元素的第一电离能由大到小的顺序 (写元素符号),其原因是
答案
(11分)(1)(1分)

(2)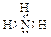 ;三角锥形;sp3杂化;配位(每空1分)
;三角锥形;sp3杂化;配位(每空1分)
(3)ls22s22p63s23p63d5(1分);Fe3+ + 3SCN- = Fe(SCN)3(2分,合理均给分)
(4)Cl>Mg>Al(1分);同一周期,随着原子序数的增加,元素的第一电离能呈现增大的趋势。但镁元素的最外层电子达到全充满的稳定结构,其第一电离能大于铝元素。(2分)
