每个圆圈代表一个试管(口),用两个圆圈相切表示试管中的两种物质在常温下能发生反应,请回答下列问题:
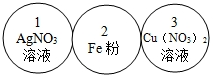
(1)用两圆圈表示4(Fe2O3粉末)、5(稀盐酸)两种物质,将4、5两个圆画到图中适当位置,并标出物质.
(2)2和3反应的现象是______;
(3)将4、5两个圆画到图中后,请写出图中某两种物质能发生复分解反应的一个化学方程式______;
(4)将1、2、3中的物质倒在一个烧杯中,充分反应后过滤,向滤液中滴加5中物质(稀盐酸),无任何现象,则滤渣中的金属有可能是.______.
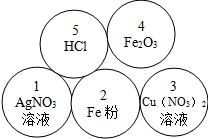
(1)根据Fe2O3粉末能与盐酸生成反应氯化铁和水,稀盐酸能与铁反应生成氢气和氯化亚铁,盐酸和硝酸银反应能生成氯化银和硝酸,绘制图片如图:
(2)2和3反应是铁和硝酸铜的反应其产物是铜和硝酸亚铁,所以其反应的现象是(黑色粉末消失)有红色固体产生溶液(由蓝色)变成浅绿色;
(3)依据酸碱盐之间的反应一般是复分解反应,所以可以写出有关复分解反应的方程式,如:AgNO3+HCl=AgCl↓+HNO3;
铁在银和铜的前面,因此铁可以和硝酸银、硝酸铜反应,滤液中加入稀盐酸,无任何现象,说明滤液中不会有AgNO3(硝酸银能与盐酸反应生成白色的氯化银沉淀),所以滤渣中一定会含有银,但反应后铁是否有剩余以及是否能置换出铜无法判断;
故答案为:(1)如图:
(2)(黑色粉末消失)有红色固体产生溶液(由蓝色)变成浅绿色;
(3)AgNO3+HCl=AgCl↓+HNO3;
(4)滤渣中一定会含有银,可能含有铁或铜或两者都有;

