金属与人类生活、生产密不可分.
(1)我国多使用铁锅炒菜,这是利用了铁的______性质;专家建议市民多食用动物肝脏、芹菜等食物,这些食物富含铁,可减少缺铁性贫血疾病的发生,这里的“铁”是指(填字母)______.
A.原子 B.元素 C.单质
(2)清末铝制艺术品至今保存完好,艺术品未被锈蚀的主要原因是(填字母)______.
A.铝不易被氧化 B.铝的金属活动性比较弱
C.铝表面的氧化膜具有保护作用 D.铝有导电性
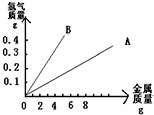
(3)如图为金属与过量盐酸反应的关系图,其中A、B两条直线分别代表镁、铁、锌三种金属中的两种.
①A代表的是(填元素符号)______;
②写出B与盐酸反应的化学方程式______.
(1)铁锅炒菜是利用铁的导热性,使煤气燃烧放出的热量传递给菜,把菜炒熟,缺铁性贫血疾病的发生中的铁是指铁这一类原子的总称,具有相同核内质子数的一类原子的总称是元素,所以缺铁性贫血中的铁是指铁元素;
(2)铝与氧气反应生成一层致密的氧化膜,这一层氧化膜使内部的铝与外界的空气隔绝,对内部的铝起到保护作用;所以铝制艺术品至今保存完好,艺术品未被锈蚀;
(3)①设生成0.2g氢气需要镁的质量为X,需要铁的质量为Y,需要锌的质量为Z,则:
Mg+2HCl═MgCl2+H2↑
24 2
X 0.2g
根据:
=24 2
解得X=2.4g;X 0.2g
Fe+2HCl═FeCl2+H2↑
56 2
Y 0.2g
根据:
=56 2
解得Y=5.6g;Y 0.2g
Zn+2HCl═ZnCl2+H2↑
65 2
Z 0.2g
根据:
=65 2
解得Z=6.5g.由图象可知B要生成0.2g氢气需要消耗B的质量大约2g多,所以B是镁;A要生成0.2g氢气需要消耗A的质量大约6g多,所以A是锌;Z 0.2g
镁与盐酸反应的反应物是镁和盐酸,生成物是氯化镁和氢气,用观察法配平,氢气后面标上上升符号;
故答案为:(1)导热;B;(2)C;(3)①Zn;②Mg+2HCl═MgCl2+H2↑.
