(12分)下表为长式周期表的一部分,其中的编号代表对应的元素。试填空。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ |
(1)写出上表中元素⑨原子的外围电子排布式 。
(2)元素③与⑧形成的化合物中元素③的杂化方式为: 杂化,其形成的化合物的晶体类型是:______________ _ _。
(3)元素④、⑤的第一电离能大小顺序是: > (用元素符号表示);元素④与元素①形成的X分子的空间构型为: 。请写出与N3—互为等电子体的分子或离子的化学式 , (各写一种)。
(4)在测定①与⑥形成的化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是: 。
(5)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质,写出元素②的氢氧化物与NaOH溶液反应的化学方程式 。
(6)元素⑩在一定条件下形成的晶体的基本结构单元如下图1和图2所示,则在图1和图2的结构中与该元素一个原子等距离且最近的原子数之比为: 。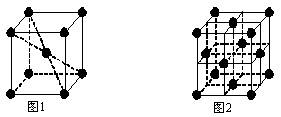
(1)3d54s1 ; (2)sp3 ;分子晶体
(3)N>O;三角锥形, CO2,或CS2、N2O、BeCl2) CNO-
(4)HF分子之间有氢键,形成(HF)n
(5)Na2BeO2
(6)2∶3,(或8∶12、4∶6)
