某火力发电厂以煤为燃料,充分燃烧后将热能转化为电能,其排出的废气中含有CO2、SO2、水蒸气等。已知SO2既能使品红溶液褪色,又能使澄清石灰水变混浊。因SO2有还原性,故还能被高锰酸钾溶液氧化而除去,无水硫酸铜与水由白变蓝。为了检验该发电厂排出的废气中的成分,用如图所示的装置进行实验。
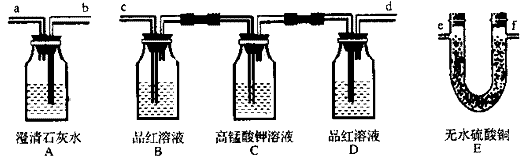
(1)仪器连接的顺序为 (填导管接口字母)
(2)根据 现象能证明有SO2存在。
(3)根据 中无明显变化和装置A中 现象证明有CO2存在。
(4)把装置E放置在最后,能否证明该废气中含有水蒸气? ,理由是 。
(5)装置B作用是 和装置D的作用是 。
(6)写出装置A中发生反应的化学方程式: 。
(1)e f c d b a
(2)B中品红溶液褪色
(3)D;澄清石灰水变浑浊
(4)不;因为A、B、C、D中的水蒸气可能随气流进入E中
(5)检验SO2气体;检验SO2是否被除尽
(6)CO2 + Ca(OH)2===CaCO3↓ + H2O