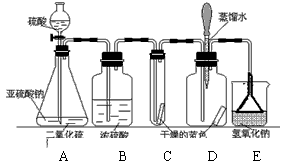
二氧化硫的性质与CO2有些相似,能与NaOH溶液反应生成亚硫酸钠和水。某化学兴趣小组的同学,欲利用下图装置和药品制取该气体,并对该气体与水在通常情况下能否发生化学反应进行探究。他们设计的探究过程如下,请你协助他们完成探究实验。
【假 设】该气体与水在通常情况下能发生化学反应,生成物可能是一种__________(填“酸”、“碱”或“盐”)。
【设计方案】先验证 能否使蓝色石蕊试纸变色,再证明该气体能否使 的蓝色石蕊试纸变色;最后验证该气体能否使 的蓝色石蕊试纸变红。
【查阅资料】你认为该兴趣小组需要查阅的资料内容应包括 (填以下的编号)。
(1)该气体是否易溶于水 (2)该气体可用什么干燥剂干燥(3)酸是否能使湿润的蓝色石蕊试纸变红
【实验】
(1)装置C内的石蕊试纸的颜色始终没有变化,这说明 。
(2)装置D中胶头滴管中的蒸馏水在该气体生成之前滴到蓝色石蕊试纸上,未见试纸发生颜色变化。当有该气体通过时,试纸的颜色变红,此现象说明 。
(3)装置E的作用是 ___________________ ,反应的方程式为 _________ 。
【结 论】原假设 。(填“成立”或“不成立”)
【假设】酸(或碱、盐)
【设计方案】水;干燥;湿润
【查阅资料】①②③
【实 验】
(1)SO2不能使干燥的蓝色石蕊试纸变色
(2)水不能使蓝色试纸变色,SO2溶于水后能使蓝色石蕊试纸变红,说明SO2溶于水生成了一种酸
(3)吸收尾气SO2; 2NaOH+SO2===Na2SO3+H2O
【结 论】成立或不成立(要与假设呼应。)

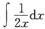 =______.
=______.