某二氧化锰样品中含有杂质炭,为测定该样品中二氧化锰的质量分数,某兴趣小组设计了如下实验方案:利用下图实验装,在一定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下反应生成CO2来进行分析测定。
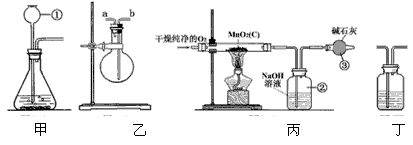
(1)仪器①的下端插在液面下是为了防止 ,如果该实验选择甲装置来制取氧气,则反应的化学方程式为 。
(2)用乙装置可用来收集和干燥气体。若在烧瓶内装入浓硫酸进行气体干燥,气体应从 端通入(选填“a”或“b”),下列气体中不能用浓硫酸干燥的是 。
A.H2 B.NH3 C.CO2 D.O2
(3)丙是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,仪器③中装有碱石灰,其作用是___________________________________。
(4)为验证装置丙中②已将CO2吸收完全,可在②与③之间加入丁装置进行证明,则丁装置中加入的试剂为
A. 浓盐酸 B. 澄清石灰水 C. 烧碱溶液 D. 浓硫酸
(5)称取8g二氧化锰样品进行实验,丙中装置②反应前后的质量差为1.1 g,计算样品中二氧化锰的质量分数为多少?
(1)产生的气体从长颈漏斗逸散到空气中;2H2O2 2H2O+ O2↑
2H2O+ O2↑
(2)b;B
(3)吸收空气中的二氧化碳,使实验数据更准确
(4)B
(5)解:设样品中二氧化锰的质量分数为x%。
C + O2 CO2
CO2
12 44
8g×(1-x%) 1.1 g
12 :44=[8 g×(1-x%)]:1.1g
x%=96.3%
答:样品中二氧化锰的质量分数为96.3%。
