金属铜和浓硝酸、稀硝酸反应的方程式如下:
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O (NO、NO2气体都是空气的污染物)
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O (NO极易与O2化合生成NO2)
工业上常用铜屑为原料制取硝酸铜,在实际生产中,需把浓硝酸用水稀释。试回答:
(1)为什么用稀硝酸而不用浓硝酸: ;
(2)从经济效益和环保角度考虑、设计制取硝酸铜的最适宜方法:
某同学设想:先将铜屑与氧气反应转化为黑色固体,再用硝酸溶解;请写出有关化
学方程式为: , 。
你认为他这种做法是否可以(简述理由) 。
(1)稀硝酸生成硝酸铜的转化率高,产生污染空气的气体少。(答对一点即给分)
(2)2Cu + O2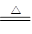 2CuO CuO + 2HNO3=== Cu(NO3)2 + H2O
2CuO CuO + 2HNO3=== Cu(NO3)2 + H2O
可以,反应效率高,不产生污染空气的气体。(答对一点即给分)
(1)用铜屑和浓硝酸、稀硝酸为原料制取硝酸铜生成了二氧化氮、一氧化氮,都属于有害气体污染了环境;观察方程式可知:Cu~4HNO3(浓),3Cu~8HNO3(稀),制备等质量的硝酸铜时消耗的稀硝酸比浓硝酸少,节约了原料;
(2)从经济效益和环保角度考虑、设计制取硝酸铜的最适宜方法是使用铜,先把铜和氧气在加热的条件下生成氧化铜,再利用氧化铜与稀硝酸反应生成硝酸铜和水,这样即节约了原料,又避免了污染;
故答案为:(1)制备等质量的硝酸铜时消耗的稀硝酸比浓硝酸少(或相同质量的稀硝酸比浓硝酸生产的硝酸铜多);
(2)2Cu+O2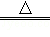 2CuO CuO+2HNO3=Cu(NO3)2+H2O;
2CuO CuO+2HNO3=Cu(NO3)2+H2O;
可以,反应效率高,不产生污染空气的气体.
