V、W、X、Y、Z五种短周期元素的原子序数依次增大,在周期表中W与V、X相邻,Y与Z相邻,X、Y同主族。Z的化合物可以发生某一反应,其离子方程式为:
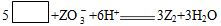 (未完成)。
(未完成)。
(1)Y、Z两种元素的简单离子的半径大小关系为 (用离子符号表示)。
(2)五种元素中分子的空间构型相同的氢化物沸点高低排列顺序为
(用分子式表示),其原因是 。
(3)V与Z单质不能直接化合生成VZ4,在催化剂作用下由VY2与Z2反应制得VZ4,其化学反应方程式为VY2+Z2→VZ4+Y2Z2(未配平)。
①写出上述化学反应方程式 。
②Y2Z2分子中,Y与Z均满足8e-结构,则Y2Z2的结构式为 。
③Y与W两种元素形成一种重要化合物A,A分子的结构如图所示:
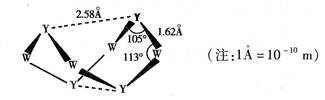
6mol Y2Z2与16mol W的简单氢化物恰好完全反应生成A、Y单质和一种中学化学中常见的盐。写出该反应的化学方程式: 。
(共10分)
(1)r(S2-)>r(Cl-)(1分)
(2)H2O>H2S(1分) H2O分子间存在氢键(2分)
(3)①CS2+3Cl2 CCl4+S2Cl2(2分) ②Cl―S―S―Cl(2分)
CCl4+S2Cl2(2分) ②Cl―S―S―Cl(2分)
③6S2Cl2+16NH3 S4N4↓+12NH4Cl+8S↓(2分)
S4N4↓+12NH4Cl+8S↓(2分)
由V、W、X、Y、Z五种短周期元素的原子序数依次增大,在周期表中W与V、X相邻,Y与Z相邻,X、Y同主族可知
| V(C) | W(N) | X(O) | |
| Y(S) | Z(Cl) |
 (未完成)。Z的最低负化合价是-1,说明Z是Cl ,Y是S ,X是O,W是N,V是C
(未完成)。Z的最低负化合价是-1,说明Z是Cl ,Y是S ,X是O,W是N,V是C(1)r(S2-)>r(Cl-),电子层结构相同的阴离子原子序数小的半径大。
(2)H2O>H2S,由于水分子间存在氢键,是水的沸点升高。
(3)①CS2+3Cl2 CCl4+S2Cl2,氧化还原反应配平。
CCl4+S2Cl2,氧化还原反应配平。
②Y2Z2分子中,Y与Z均满足8e-结构,共价键成建理论硫原子存在两个单电子,氯原子存在一个单电子,可知Cl―S―S―Cl
③6S2Cl2+16NH3 S4N4↓+12NH4Cl+8S↓氧化还原反应配平。
S4N4↓+12NH4Cl+8S↓氧化还原反应配平。